撰文:倪楠
突破技术
美国即将批准首个基因治疗技术,更多的基因疗法正处于开发与批准的进程中。
重要意义
很多疾病都是由单个基因突变导致的,新型的基因疗法能够彻底治愈这些疾病。
技术成熟期
现在
主要研究者
-Spark Therapeutics
-Bio Marin
-Blue Bird Bio
-Uni Qure
-Gen Sight Biologics
基因治疗是人类医疗史上伟大的革命,因为它向最困难、最致命而且还有可能贻害后代的一大类疾病发起了有效的冲击。虽然真正进入市场发挥治疗作用的基因疗法仍然屈指可数,但是已经获得了初步的成功。
“修复控制系统”
我们的身体包含10万亿~100万亿个细胞,比银河系中的恒星和行星的总数还多。每个细胞都像一个工厂车间,在这些车间中,有负责控制的中央操控系统,有负责运输的传送系统,还有负责生产的流水线。每个工厂车间不仅要生产供自己生存的产品,保持结构和功能的稳定,还要配合其他车间,通过合作让整个人体正常运转。比如,肝脏中的细胞车间需要生产能够分解有毒物质的产品,大脑中的细胞车间需要发电互相通信,而头皮上的车间则负责生产、聚集头发。
在每个细胞车间中,最为关键的部门是中央操控系统。因为这个部门相当重要,所以处于一个专门辟出的“单间”里。在那里,“控制台”可以根据设定好的程序发出各种指令,通过传送系统运输到控制室外面,让流水线在合适的时间生产正确的产品。如果整个过程中的任何一步出了问题,我们就有可能生病。
如果用生物术语来说的话,控制室就是细胞核,而控制台发出指令所依据的程序就是我们的遗
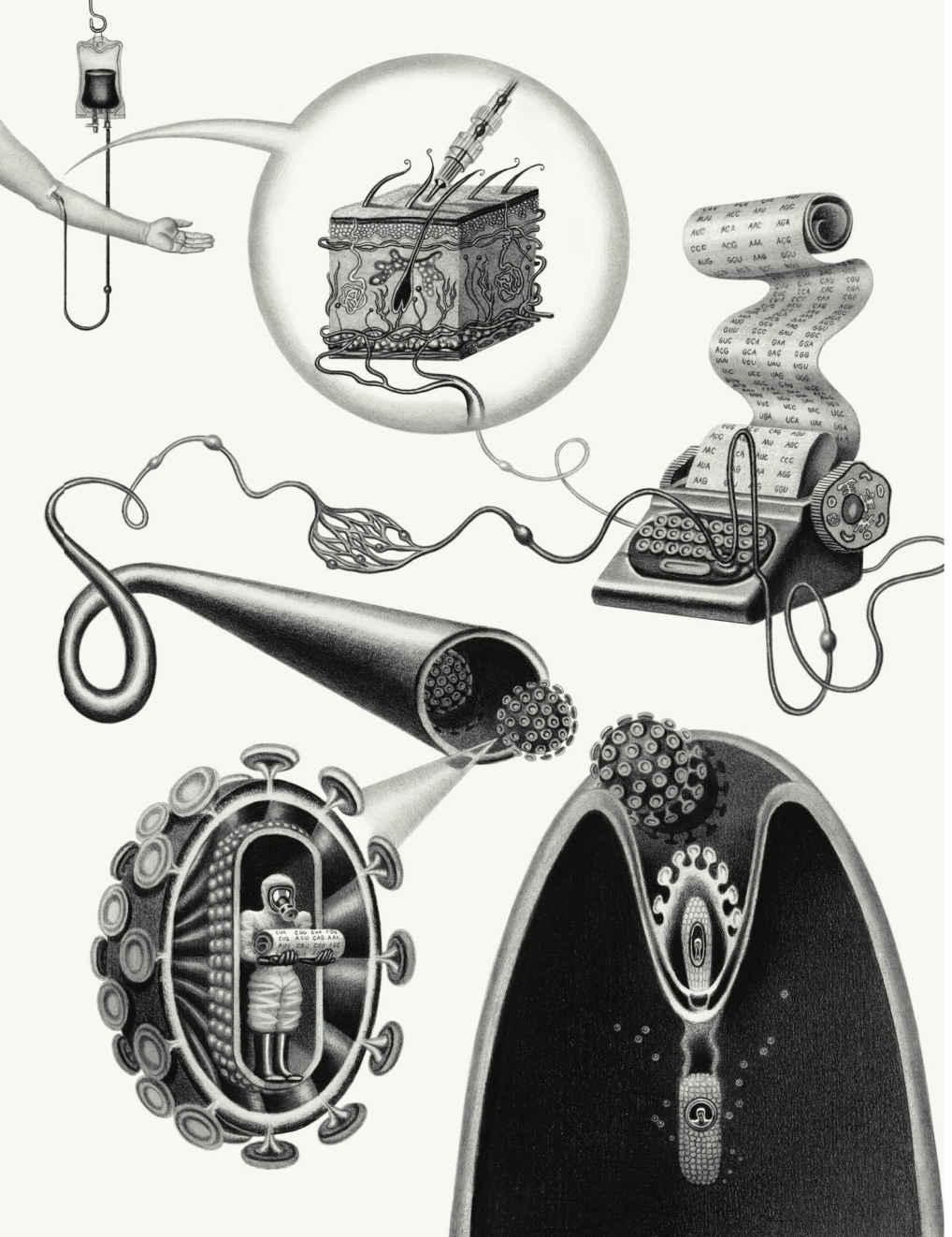
基因疗法时间线

20世纪60年代
当科学家发现一些酶可以在试管里切割连接的DNA序列以后,就开始考虑基因疗法的可能性。

20世纪70年代
科学家开始在实验中用病毒向动物体内导入新基因。

1990年
1992年,一个4岁的小患者(图中右下角)在接受基因治疗后战胜了SCID(重症联合免疫缺陷)——一种让人无法抵御感染的遗传性疾病。不过一些接受了不同基因疗法的患者后来得了白血病。

1999年
18岁的Jesse Gelsinger成了基因治疗临床试验的第一个牺牲者。
传物质,也就是DNA。可以想象,如果控制室外的东西出了问题,会比较容易修复。因为核心的控制程序仍然是正确的,所以故障很可能只是临时性的,只要控制台再发一次正确的指令就好了。然而,如果控制程序,也就是我们的DNA出现了错误,就会有很大的麻烦,因为中央控制系统会持续不断地发出错误的指令。更糟糕的是,错误的控制程序不仅会让人生病,还会被遗传给下一代。这也是几乎所有遗传病都无法被根治的原因,现有的药物只能减轻症状而已。即使这样,病情也会逐渐加重并最终积累到致命的程度。
基因疗法的目的,是希望可以修复错误的中央控制程序,也就是突变以后的DNA。不过,要完成这一目标难度很大。首先,因为DNA很重要,所以细胞对它施加了重重保护,让任何试图改变它的药物难以接近。而且对DNA的改变如果出了差错,会造成严重的后果,如细胞死亡或癌变。
最终,科学家还是找到了方法。在自然界中,有一种天然的DNA载体,就是病毒。病毒的结构极其简单,所以单靠它自己不能完成任何生命活动。它们所做的,只是把自己携带的遗传物质注入细胞里,变成细胞自身遗传物质的一部分,然后让细胞帮助自己完成合成和装配的工作。所以,病毒的遗传物质就好像黑客程序,可以通过非正常手段进入戒备森严的控制室,并进入核心控制系统,让控制台发出新的指令,命令细胞车间开始为复制新病毒服务。
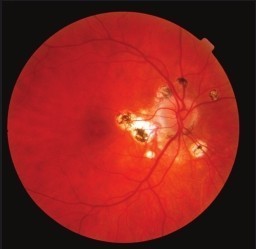
2007—2008年
莱伯氏先天性黑矇症(Leber's Congenital Amaurosis,一种遗传性视网膜疾病)患者在接受了基因治疗后视力得到改善。不过数年后,研究人员在《新英格兰医学》上发表文章指出,有些病人的视力又出现了退化。

2012年
欧洲药品管理局批准了首个治疗遗传疾病的基因疗法:Glybera。这一疗法用来治疗脂蛋白脂酶缺乏症,该疾病可以导致脂肪在血液中积累。

2016年5月
英国监管机构批准了Strimvelis,这是第二个在欧洲获批的基因疗法,可以治疗SCID。

2017年或2018年
美国可能将首次批准治疗遗传疾病的基因疗法。
虽然病毒经常让人生病,不过如果把病毒自己的基因换成能治疗遗传疾病的正常基因,就像是把黑客变成了偷偷潜入系统并修复错误的正义黑客。目前,绝大多数处于临床试验阶段的基因疗法都以病毒为载体。首先,科学家会选择那些天生温和的病毒;随后,他们还会对病毒进行基因改造,去掉那些不必要的基因,只保留疗效基因和供病毒把疗效基因插入人体基因组的DNA序列。
然而,虽然这些原理说起来很简单,但是基因疗法在过去几十年里走过的道路却无比曲折。
曲折与失败
早在1972年,基因治疗的概念就被提出了。两位美国科学家Teodore Friedmann和Richard Roblin在《科学》杂志上撰文表示,基因疗法将会成为有用的医疗技术[1]。那时,人类才刚刚能够修饰哺乳动物细胞的基因,但对整个细胞的生物过程以及很多疾病的分子机理还不清楚,所以Friedmann和Roblin反对立刻进行人类基因疗法的临床试验。
他们的观点没有错。此后,科学家仍然在基础科学领域丰富知识。他们一方面需要鉴定出具体的基因突变与某个疾病的因果关系,另一方面也要改进修饰基因的技术,让其变得更稳定,提高其可预测性。

直到1990年,第一个临床试验才被批准展开。此后的9年里,也有一些零星的研究陆续展开。1993年,一个婴儿在出生前就被诊断出患有免疫疾病,他的免疫系统不能工作,出生以后很快就会死亡。他的父母已经因为同样的原因失去了一个孩子,所以希望尝试一些新的疗法来冒险挽救他。加州大学洛杉矶分校的Donald Kohn教授决定采用基因治疗的方法。当孩子出生以后,他和同事立刻抽取了胎盘和脐带中的干细胞,并将其与携带正常基因的逆转录病毒混合。在逆转录病毒把正常基因转入干细胞以后,Donald Kohn把干细胞注射回婴儿的体内[2]。在随后的4年时间里,病人虽然仍然需要接受药物注射,但是他的体内已能合成本来不能合成的酶。虽然4年后病人体内的酶消失了,但这仍然说明基因治疗在某一个时间段内产生了效果。
到了2000年,全世界大约有4000名患者参与了500多个基因治疗的临床试验。
然而,就在基因治疗初露曙光之际,几次巨大的挫折却让基因研究的前景蒙上了阴影,其中就包括了《麻省理工科技评论》的文章中提到的Jesse Gelsinger事件。
Jesse Gelsinger是一名出生在美国亚利桑那州的少年。他天生就缺少一种正常的消化酶。这种消化酶可以代谢蛋白质的消化产物“氨”。随着有毒的氨在体内慢慢积累,病人很快会有死亡风险。虽然这种疾病在出生时就能致人死亡,但Gelsinger体内有一部分细胞是正常的,这让他可以通过低蛋白饮食和定期吃药来控制病情。
不过,为了尽力让他过上正常人的生活, Gelsinger的父母还是决定让他参加一项由宾夕法尼亚大学的科学家主持的临床试验,尝试用基因治疗的方法来彻底治愈此疾病。在此之前,科学家已经在小鼠、猴子、狒狒和数个人类病人身上尝试过将腺病毒作为载体的治疗方法,他们只发现了类似感冒的轻微副作用,并且症状会自己消失——类似的治疗曾经导致参加实验的猴子因免疫反应而死亡,不过科研人员认为他们已经修改了作为载体的病毒,因此不会再出现这样的副作用了。
医生们把正常的消化酶装到腺病毒里,然后向Gelsinger的肝脏里注射了10万亿个这样的病毒。然而,悲剧发生了。虽然有很多带着治疗基因的病毒载体确实进入了肝脏细胞,但也有一些感染了负责身体保卫工作的巨噬细胞。当外来的病原体入侵人体的时候,巨噬细胞可以召集各种各样的免疫细胞对外来者发起攻击。最终,这些误以为遭到了感染的巨噬细胞在Gelsinger体内发起了一场暴风骤雨般的免疫反应,不分敌我的免疫系统最终摧毁了Gelsinger的身体。在接受治疗的4天后,Gelsinger因免疫反应导致的多器官衰竭而死亡。
Jesse Gelsinger事件在美国社会造成了巨大的反响,相关的医学技术和医学伦理争议不停地在媒体头条上出现。尤其是科研团队没有告知Gelsinger的父母在动物试验过程中有猴子死亡一事,从而引发了潮水般的批评。事件发生以后,主持研究的宾夕法尼亚大学教授James M.Wilson受到了FDA(食品药物管理局)的调查,并被发现存在违规行为。而美国的基因治疗研究也一度陷入停滞[3,4]。
在欧洲,也出现了类似的情况。2000年,一些患有重症免疫缺陷(SCID)的幼儿接受了基因治疗的临床试验。患有这种疾病的幼儿天生没有免疫能力,不能对抗哪怕是非常轻微的感染,所以只能终生生活在经过严格消毒的塑料室里,因此又叫“气泡宝宝”。患者不仅无法过上正常的生活,而且还会因为意外的感染在很小的时候就失去生命。
研究人员这次利用逆转录病毒作为基因载体,植入正常版本的基因,再把这些运载着治疗基因的病毒注射到病人体内。在病人体内,逆转录病毒会把正常的治疗基因插入人类自己的基因组里[4]。

基因治疗一开始取得了很大的成效。病人体内也产生了新的免疫功能。但是在几年后,情况却急转直下。在接受了免疫疗法的20个婴儿中,有5人得了白血病,其中1人因此死亡。2003年, FDA暂时中止了所有利用逆转录病毒进行基因治疗的临床试验。
很久以后,科学家才查明了原因。逆转录病毒在把基因插入到人类基因组的过程中非常随意,它们有时会把基因插到原癌基因LMO2附近。原癌基因是指那些维持正常的生理功能,但是一旦突变就会致癌的基因。通过基因疗法插入的基因意外地激活了LMO2,再加上一些其他的基因突变,让白细胞不受控制地大量增殖,最终导致病人得白血病[5]。
技术更新
多次的挫折在表面上让基因治疗的临床应用产生了停顿,但却不完全是一件坏事。因为这让研究人员能够暂时从商业化的狂热中冷静下来,开始从头仔细地审视相关的基础科学研究,并试图从根本上改进基因治疗的方法。
在失败的临床试验中,病毒载体的失控成了一个重大的问题。一方面腺病毒可能会引发强烈的免疫反应,另一方面逆转录病毒又会激活失控的原癌基因。因此,科学家开始着手为治疗基因寻找更好的运载工具。
最终他们找到了一类温和的病毒:腺相关病毒。这类病毒有时候会感染人类和其他灵长类动物,但是不会引发疾病,因此免疫系统也不会产生剧烈的反应。而且,经过进一步的研究,科学家已经剔除了天然腺相关病毒中96%的基因组,进一步降低了感染致病的风险。此外,腺相关病毒不会把基因插入人类自己的基因组里,所以致癌的风险也不大。
腺相关病毒还有一个重要的特点:它有很多不同的亚种(术语叫“血清型”)。每种亚种的病毒,其表面的蛋白质都不相同。在进入人体后,这些蛋白质像钩子一样钩住人体细胞的表面,然后病毒就可以把自己携带的治疗基因注入细胞。因为钩子不同,所以病毒可以进入的细胞类型也不同。这就让医生可以为某种特定的疾病找到“专业”的腺相关病毒,不影响其他类型的人体细胞。而且,研究人员还可以通过DNA改组技术(DNA Shufing)改变或设计新的腺相关病毒。
利用这个新发现的“武器”,基因治疗终于取得了重大的进展,第一次通过了临床试验阶段,进入了市场。
消除血液中的“奶油”
为什么人的血液是红色的?因为红光不会被红血球中的血红素吸收,而是会被反射出来。但是,如果得了某些疾病,改变了血液成分,血液就不再呈现红色,看上去会显得有些发白。脂蛋白脂酶缺乏症(Lipoprotein Lipase Defciency)是一种罕见的疾病,大约每100万人中只有1人会得此病。病人的体内缺乏一种必需的酶来分解饭后在血液中循环流动的脂肪颗粒。用蒙特利尔大学教授丹尼尔 · 高德特(Daniel Gaudet)的话来说,得了这种病就相当于血液中有了10%的“奶油”。
这些额外的“奶油”会对健康造成非常严重的损害,不仅会导致急性胰腺炎的反复发作,还会产生腹部疼痛和其他慢性的健康问题。因为患者的遗传物质发生了改变,所以只能通过坚持吃极度低脂的饮食来缓解症状,且没有其他有效的治疗方法。一般来说,医生会建议病人每天摄入的脂肪不超过20克,这大概相当于100克肉食或500克全脂牛奶中的脂肪含量,病人受到的饮食限制可想而知。2012年11月2日,欧盟正式批准了荷兰生物技术公司Uni Qure 的基因疗法Glybera。Uni Qure公司位于阿姆斯特丹,是阿姆斯特丹大学技术转化的产物。Uni Qure长期以来一直在努力地让基因疗法进入临床应用。Glybera的上市绝非一帆风顺,因为之前的诸多事故,仅在一年之内欧盟人用药品委员会(Committee for Medicinal Products for Human Use)就三度拒绝了Glybera的申请,并对其安全性和有效性提出质疑,直到Uni Qure公司确实提交了足够多的证据以后才打开了绿灯。直到2012年7月20日, Glybera疗法才获得了欧盟人用药品委员会的肯定,而欧盟此次的批准消除了这一疗法进入市场的最后障碍。
从1990年基因疗法首次进入临床试验到现在,已经20多年过去了。而西方国家在此之前还从来没有批准过任何一种基因疗法上市。
Glybera可以提供正常版本的脂蛋白脂酶基因,这些基因在体内会合成没有缺陷的酶,分解血液中的脂肪颗粒,从根本上缓解病情。根据Uni Qure公司的说法,病人只要经过一次治疗,就能维持至少数年的疗效。
Glybera利用腺相关病毒装载正常的基因。在接受治疗的时候,医生会把这些病毒载体分成几次注射到病人的大肌肉群里,比如腹部和腿部。不过腿部肌肉往往是第一选择,不仅是因为它面积较大,容易注射,还因为腿部活动量大,可以及时吸收能量。
然而,虽然Glybera在技术上成功了,但是在商业上却失败了。在Glybera刚上市的时候,病人需要花费160万美元才能接受治疗。脂蛋白脂酶缺乏症是一种极为罕见的疾病,发病率只有一百万分之一,所以Glybera在欧盟的市场只有100多人。另外,脂蛋白脂酶缺乏症不是致死性疾病,虽然它会导致因高血脂引发的胰腺炎和糖尿病等并发症,但是患者可以通过严格控制饮食来延缓并发症的发生,这让接受这种昂贵的治疗的人群又减少了一些,而且很多时候保险公司也不愿意为非急性病支付太多的账单。即使国家福利制度愿意帮助病人承担部分费用,当治疗更常见疾病的基因疗法上市以后,如果价格还不下降,势必会成为整个社会沉重的负担,从而变得难以推广。最终, Glybera只在欧洲治疗了一名病人,而且根本没有在美国上市。Uni Qure公司也把注意力转向了其他可能被基因疗法治愈的疾病,如血友病。
商业与政策的双重挑战
在Glybera之后,大量的基因治疗方法如雨后春笋般出现。美国和欧洲也出现了很多生物技术初创企业专门研究基因治疗技术,比如美国的Spark Terapeutics和Bluebird Bio,以及欧洲的Gen Sight Biologics。现在,有数千种基因疗法正在接受临床试验。2016年,欧盟批准了葛兰素史克的基因治疗方法Strimvelis,这种疗法可以治疗先天性的免疫缺陷症,也是首个用于儿童治疗的基因疗法。在美国,比较有前景的基因疗法是Spark Terapeutics开发的SPK-RPE65,用来治疗遗传性视网膜营养不良。患有这种疾病的人双眼感光功能会慢慢消失,并最终失明。
然而,虽然新的疗法频频出现,看起来十分热闹,但是基因疗法的价格却始终降不下来。预计SPK-RPE65的价格是每只眼睛50万美元,两只眼睛加起来就有100万美元。尽管葛兰素史克一再强调不愿意给药物标上天价,而且“公司也不会依靠基因治疗来获取利润”,但最终Strimvelis的价格仍然被定在了59.4万欧元,这也让它成为史上最贵的一次性药物之一。
为什么基因疗法的价格这么昂贵?一方面是因为高企的研发费用,另一方面则是因为很多基因疗法针对的是罕见疾病,因此市场总额有限。Uni Qure在研发Glybera时,甚至很难找到足够多的接受临床试验的志愿者。当时欧盟表示,Uni Qure需要报告342名志愿者的试验结果,但是全欧洲的病患加起来也才200多人。Glybera的总研发费用大约是1亿美元,这些费用要由200多人大小的市场分摊,每个人所需付出的代价可想而知。
葛兰素史克的Strimvelis也面临类似的困境。该疗法针对免疫性疾病ADA-SCID。这种疾病的患者因为没有免疫系统,基本很难活过1岁,每年欧盟只有15名患者被确诊。

如何让新的基因治疗药物不像Glybera那样成为商业灾难,成了制药公司和风险资本面对的一个重要问题。首先,制药公司和保险公司一起制定了“按效付费”的机制,即如果基因疗法没有产生疗效,治疗机构将全额退款。此外,基因治疗公司正在建立一个“结果导向体系”,在此体系下,制药公司可以证明一次性的昂贵价格其实比终身治疗给社会和病人带来的负担更小。制药公司会长期跟踪病人的预后,只要疗法仍然有效,接受治疗的病人就可以定期付费。

另外,还有研究人员建议制药公司可以通过美国的孤儿病法案(orphan drug act)规定的退税优惠用于降低药物价格。该法案规定,如果制药公司为病患小于20万名的疾病开发药物,可以获得一些税收方面的优惠政策。
不过,归根结底,降低基因治疗的药物成本还需要技术进展的支持。科学界需要找到更精确、更自动化的方法来寻找新的疗法,从而降低药物开发的成本,从源头上解决药物昂贵的问题。基因治疗的成本问题需要科学界、制药公司、保险公司、非营利组织和政策制定者共同解决,毕竟发明疗法的目的是治愈病人。也许就如葛兰素史克的发言人Anna Padula所说:“不久以后,工业界和资本界终会找到消化药物定价的新玩法。”
中国的基因疗法:起早赶晚
中国很早就开始在基因治疗领域开展临床试验,也成为第一个批准基因疗法的国家。除了对这个领域的重视以外,宽松且不够完善的临床试验监管系统也是中国起步早的原因之一。
1998年年初,在美国和日本留学多年的彭朝晖携带专利权中属于自己的基因技术回国,创办了生物技术公司赛百诺。赛百诺公司主要利用重组的腺病毒向癌症病人的体内输送抗癌病毒p53。当细胞出现可疑的癌变时, p53基因可以“卡住”细胞的分裂过程,还能启动程序让细胞自我毁灭,因此成为防止细胞癌变的“守护神”。然而,有时p53也会发生突变,失去功能,这样细胞就特别容易癌变。此外,如果p53发生突变,还有可能让癌细胞抵抗化疗和放疗。所以,传统的癌症疗法相当于起了一个人工选择的作用,把容易杀死的癌细胞杀光,却让不容易杀死的癌细胞越来越多,最终变得无药可治。
赛百诺的科学研究团队利用腺病毒,把正常版本的p53导入有缺陷的癌细胞里。根据后来的临床试验结果论文显示,实验结果不仅可以让癌细胞重新对放疗、化疗敏感,有时甚至还能直接终止癌细胞的分裂周期。
p53是被研究得最广泛的癌症相关基因,而腺病毒也是当时最常见的基因治疗载体。所以p53+腺病毒治癌症的想法不可能没人想到。事实上,已经有很多国家都做过相关的试验,但临床试验基本上以失败告终。比较著名的例子是美国的生物技术公司Introgen发明的基因疗法Advexin。尽管Introgen公司号称成功地完成了三期临床试验,但负责审批药物上市的FDA却不买账。反复拉锯之后,FDA甚至拒绝审查Introgen提交的申请。最终,Introgen公司的股东认为他们被公司骗了,群起而攻之,公司则直接破产清算,成了生物技术泡沫的一个注脚。
在中国,监管就宽松多了。基因治疗药物“今又生”甚至没有经过三期临床试验就上市了。根据彭朝晖的解释,这么做符合当时的临床试验规范(GCP):Ⅰ期临床试验检测安全性,Ⅱ期试验检测有效性,Ⅰ、Ⅱ期试验通过后即可批准生产,Ⅲ期临床试验是药品上市以后的过程。一般来说,前两期临床试验的参与者人数不多,而Ⅲ期临床试验需要大量的治疗病例,所以尤为重要。对此,彭朝晖的解释是实际做的病例数比提交的病例数要多。最终,北京肿瘤医院张珊文和福建省肿瘤医院潘建基联合组织了Ⅲ期临床试验,直到2009年才把结果发表在《临床肿瘤学杂志》(Journal of Clinical Oncology)上[6]。好在“今又生”没有在后续的试验和临床治疗中引发安全事故,而且似乎在统计上也确实有疗效。
不过,赛百诺却在公司治理和资本合作上遭到了致命的打击。
在上市前,作为有可能成为世界上第一个上市的基因疗法的公司,赛百诺的实验室研究接受了国家提供的大量补助,资金超过5000万元。甚至连Ⅲ期临床试验的资金也是由国家的973项目提供的。在开始走向市场之后,国家科研经费很难支持扩建产能、市场推广等企业方面的费用。而“今又生”在市场上的反响也不及预期,它的价格太贵,又不在医保体系中;医生对这种操作陌生的全新方法也有顾虑——根据著名科学记者贾鹤鹏的观点,这里还有医疗腐败和医患关系紧张等复杂因素的干扰。2007年,“今又生”的销售额只有576万美元。
就在这个时候,湖北同济奔达鄂北制药公司向彭朝晖表达了合作意向。这家公司并没有高端的技术,主要靠维生素和原料药发家,利润率比较低。需要核心技术的奔达和需要资本的赛百诺很快达成了合作。一开始,奔达计划出资5000万元购买赛百诺10%左右的股权,但是因为赛百诺的两家占40%的国资股东希望退出,所以就把股权转让给了奔达。最后奔达占了赛百诺60%的控股权。于是奔达的创始人万宜青、徐卫夫妇进入了赛百诺的董事会。
在资本市场较为发达的今天,很容易发现这种投资方式的问题:一个较为传统的企业以财务投资的形式入股前沿新兴技术行业,却占据了绝大多数股份,控制了公司的经营和发展。根据《中国企业家》的分析,此时的赛百诺已经为日后的纠纷埋下了病根。一方面,控股股东派遣一对夫妇占据了董事会三席中的两席,其中一人担任总裁;另一方面在董事会处于弱势地位的创始人则掌握了生产和研发的命脉,但同时却是公司的法人代表和董事长。
双方很快就发生了激烈的冲突。彭朝晖认为万宜青和徐卫不尊重技术员工,大量解雇他们认为成本过高的科研人员。而万宜青和徐卫则认为彭朝晖完全不懂企业管理,不尊重董事会的决议,甚至背着董事会自行寻找外部投资。2008年,“今又生”的销售额只有2007年的一半;2008年6月11日,国家食品药品监督管理总局正式吊销赛百诺的GMP证书,这意味着此后的“今又生”的生产是非法的,赛百诺的内斗开始进入白热化。徐卫认为这次事件是彭朝晖主动举报导致的[7]。在双方的矛盾彻底公开后,彭朝晖离开了赛百诺,但声称自己有“今又生”的知识产权。双方的法律纠纷持续了近10年,经历了深圳中院一审、广东省高院驳回上诉、最高检向最高法抗诉、广东省高院再审等多次审判和上诉。最终,广东省高级人民法院在2015年做出终审判决,裁定涉案的专利属于赛百诺公司。
除了法律纠纷造成的损耗外,赛百诺在很长一段时间里仍然没有展示出足够多的临床试验数据。公司曾尝试在印度申请上市,但也承认这一疗法根本不可能进入审批更加严格的欧洲和美国的市场。这让赛百诺的市场表现一直都不理想。而同一时期,美国出现了很多新的基因疗法技术公司,也开始针对很多不同的疾病展开临床试验。中国的基因治疗市场化“起了个大早,却赶了个晚集”。
中美环境差异
美国市场决定了生物技术初创公司可以专注于基因疗法的研发,甚至只研究一种产品。它们可以从多个渠道获得研发资金,即使没有盈利也可以上市公开募资。
到2016年年底,至少有12家专注于基因治疗的公司在美国上市。除了前文提到的Uni Qure、Spark Terapeutics和Bluebird Bio,还有用基因疗法治疗罕见肝脏疾病(如Jesse Gelsinger得的鸟氨酸氨甲酰基转移酶缺陷症)的Dimension Terapeutics、治疗脊髓性肌肉萎缩症等罕见神经系统遗传疾病的Avexis,以及治疗家族性高胆固醇血症等遗传代谢疾病的Regenxbio。
2016年2月,由基因编辑技术CRISPR的发明者Jennifer Doudna和张锋创办,比尔·盖茨、Google Ventures等投资的Editas Medicine在纳斯达克上市。Editas Medicine明确地向投资者表示,公司目前只是拥有基因编辑技术的专利授权,离商业化的产品还有相当一段距离。但这并不妨碍投资人的热情,截至2017年3月15日,Editas Medicine的市值达到了9.03亿美元。
目前,纳斯达克有至少6家基因治疗企业的市值超过3亿美元,如Bluebird公司的市值为40.06亿美元、Spark Terapeutics公司的市值为18.5亿美元、Regenxbio公司的市值为5.38亿美元。但这些公司的利润全部为负,因为它们的产品全部处于临床试验阶段,还没有进入市场。
因为中国的资本市场对营收的要求更高,而且中国在技术向临床转化的过程中存在监管和法律上的不确定因素,所以在美国基因治疗初创公司百花齐放的情形在中国很难出现。很多对基因治疗感兴趣的初创公司只能通过各种相关的其他业务增加收入。2014年,由清华大学孵化成立的云生基因正在试验用基因编辑技术治疗癌症和白血病,但公司同时也需要开发和销售生物试剂以及向科研机构提供合成生物学方面的商业服务。
和美国的FDA不同,目前中国的监管部门尚未形成一个专业评估基因疗法的团队。而这样的团队本身也需要接受锻炼,在审批了一定数量的基因疗法申请后才有可能出现。此外,中国需要更多可以接受更长回报周期的资本。
在美国,很多基因疗法的临床试验和审批由患者的强烈需求推动,基因治疗的市场规模已经形成共识,相关的技术也已经成熟到了一个临近爆发的临界点。中国和美国相比,除了技术之外,欠缺成熟规范且有经验的法律和市场监管,也缺少对生物医学和基因治疗有深入理解的风险资本。如果中国出现几个上市的基因疗法,让监管和资本有了可以直接参考的案例,可能会像美国那样迎来一波市场的爆发。
专家点评
谢震
清华大学信息科学与技术国家实验室研究员,“青年千人计划”获得者,博士生导师。
2004年,我国批准了世界上首个基因治疗药物重组p53腺病毒注射液(今又生),用于治疗头颈部鳞癌和其他恶性肿瘤;2012年,欧盟委员会批准了西方世界首个基因治疗药物Glybera,用于治疗罕见遗传病脂蛋白脂肪酶缺乏症(LPLD);2016年,欧盟委员会又批准了用于治疗重度联合免疫缺陷病(ADA-SCID)的基因治疗药物Strimvelis;2017年,美国生物技术公司Spark Terapeutics研发的用于治疗由PRE65基因突变引起的遗传性视网膜疾病(IRD)基因治疗药物Voretigene Neparvovec有望获得FDA批准在美国上市。基因治疗2.0时代即将来临!基因治疗的想法自20世纪60年代提出以来,经历过20世纪90年代末的阵痛,终于迎来了真正的春天!
基因治疗2.0与之前的技术相比,主要在于采用了20世纪更加安全的递送机制。目前的基因治疗药物,比如Voretigene Neparvovec以及Bio Marin Pharmaceutical公司研发的用于治疗A型血友病的BMN270,采用的是腺相关病毒(AAV)运载相关治疗基因。该病毒与其他病毒载体相比,安全性好,免疫原性低,基本不引起机体的免疫排斥和炎症反应,插入基因组和潜在的致瘤性的风险小,并且具有较强的靶向性。除此之外,具有低免疫原性且能够将携带的基因药物插入到宿主基因组中稳定表达的慢病毒(Lentivirus)载体是另一种安全的递送载体,比如Bulu Bird Bio公司研发的Lenti Globin BB305基因治疗药物就是利用改良后的慢病毒将正常的β球蛋白基因送入人体,来治疗由β球蛋白基因缺陷导致的重度β地中海型贫血病。
除了更加安全的递送机制,基因治疗2.0时代还具有另一个技术优势——精确地对基因组进行编辑。基因组编辑可以定点修复遗传突变,从根本上阻止遗传疾病的产生,也可以对靶向位置进行基因序列的插入/删除,扩展了传统的“缺什么补什么”的基因治疗策略。基因组编辑技术曾在2014年当选《麻省理工科技评论》10大突破性技术。最近,研究人员开发出了迄今最小的CRISPR-Cas9系统,并通过腺相关病毒运载到小鼠的眼部进行基因编辑,用以修饰引起失明的一个基因。另外,基因组编辑技术已经开始用来改造免疫细胞,治疗自身免疫系统疾病以及癌症的临床试验也在陆续进行。可以预见,在不久的将来,基因治疗会成为多种罕见遗传病和癌症的有效治疗手段。
专家点评
茅矛
华大基因股份有限公司首席科学官。
基因作为控制生物性状的基本遗传单位,控制着生物的出生、疾病、衰老以及死亡等过程;当基因出现异常或遭到破坏,就会导致疾病的发生。基因治疗就是通过治疗“坏掉”的基因,让它们表达出正常的功能蛋白,实现减缓或从根源上治愈疾病。然而这种看似简单的治疗理念,实践起来却不那么容易,接踵而至的悲剧让基因治疗进入了寒冬。经历数十年的迂回与曲折,基因治疗技术的一些关键性难题得以突破,基因疗法升级至2.0版,治疗遗传性疾病已不再是一种奢望。
2012年,荷兰Uni Qure公司研发的基因药物Glybera由欧盟审批上市,开启了基因疗法2.0新时代;2016年,葛兰素史克公司的基因治疗药物Strimlevis在欧洲被批准上市,成为基因疗法走向临床市场的又一个里程碑。Spark Terapeutics公司开发的针对渐进式失明的基因治疗方法或将成为美国首个批准的基因治疗技术。近期,法国研究者在《新英格兰医学杂志》上发表文章称,其使用基因疗法成功治愈了一名患有镰状细胞贫血症的患儿。另外一些临床试验和动物模型试验显示在治疗帕金森症、阿尔茨海默症和癌症上效果显著。这意味着基因疗法的研究和应用领域从罕见病向常见遗传病及复杂疾病拓展。
尽管目前全世界只有为数不多的基因疗法获得了批准,但从2016年基因治疗技术所取得的几项不容忽视的重大进展以及少数治疗领域初步实现商业化来看,基因治疗在慢慢地引领着一场革命性的全球医疗变革。这种变化主要体现在从“对症”治疗向对“基因”治疗的模式转变,经验性和传统治疗模式在未来或许被逐步打破,取而代之的是精准的预防和诊断,最终实现精准的个性化治疗。华大基因其实一直在为“对因”治疗提供诊断依据,通过规模化测序与云计算分析,不断积累健康大数据,提高对疾病风险的预测和病因分析的准确性。未来,基因疗法不再局限于罕见病、遗传病,甚至有望革新癌症的治疗。
在精准医学时代,基因测序技术的进步和大数据分析工具的出现为基因治疗提供了一条捷径。但不可否认的是,基因疗法在技术研发和产业化的过程中仍面临技术门槛高、治疗费用昂贵、伦理局限等诸多问题,用一句简单的话概括:希望与困难同在,机遇与挑战并存。
专家点评
田埂
元码基因联合创始人,曾任清华大学基因组与合成生物学中心主管,华大基因华北区第一负责人,天津华大创始人、总经理,深圳华大基因研究院研发副主管。
早期基因疗法失败的原因部分是源于其递送机制,因为新的遗传物质(改造基因)以及将其携带至细胞的载体病毒,被错误地递送到基因组的其他位置,这会激活患者体内的某些致癌基因,或者引起患者免疫系统的过度反应,从而导致多器官功能衰竭以及脑死亡。
人类大量的疾病都是由于DNA发生突变引起的,科学家数十年来一直在研究通过基因治疗来改善人类的健康。然而在开始时,基因疗法带来的失望远大于希望。1999年,一名18岁的肝病患者杰西·基辛格(Jesse Gelsinger)在一项激进的基因治疗实验中死亡,使得整个基因疗法领域的发展停滞不前。
对于改造生物的遗传性状,人类其实已经有千年的历史。通过选择性培育,我们强化了动植物中有用的特性,比如我们培养出了好看的金鱼、产量更高的小麦等。虽然我们很擅长做这类事情,但实际上还没有明白这是怎么回事。直到后来发现这一切都是基于DNA分子,它包含了生物所有的遗传信息,是生物的一张说明书。
基因治疗2.0时代基于新的基因编辑技术,极大程度地改善了这些问题,基因治疗也将迎来曙光。两种遗传性疾病的基因疗法:治疗SCID病的Strimvelis,以及治疗Lipoprotein Lipase Defciency病的Glybera,已在欧洲获得相关管理部门的批准。
不可否认,在技术层面上基因治疗2.0仍存在脱靶,同源重组条件要求苛刻,去除简易而修改困难,难以控制修饰后蛋白表达量等诸多问题。但这次飞跃已经可以通过引发其他技术的变革来实现更重要的应用。比如CAR-T治疗2.0利用基因编辑技术,可以通过改变回输细胞的免疫排斥性,大大降低其应用范围和成本,有着非常深远的影响。
永久地改变一个病人的DNA序列,从而彻底消除该疾病。随着技术的发展,相信基因治疗这把“上帝的手术剪”最终会真正地在人类未来的健康领域发挥极其重要的作用。
专家点评
孙隽
北京金准基因科技有限公司副总裁。
DNA承载着生命的密码,使得物种得以延续。如果说DNA的发现让人类能够读懂“上帝的密码本”,那么基因治疗是人类开始根据这个神奇的密码本将错误的编码修正。从广义上来讲,所有在DNA水平所采取的治疗手段都可以称为基因治疗,可以是体内对个人的基因进行纠正、置换、增补、失活,也可以是体外引入外源的具有正常基因的细胞,甚至可以重编码患者的免疫细胞,使得其具备针对性的防御功能。目前,基因治疗技术已在治疗肿瘤、罕见病等领域取得了可喜的进展,虽然目前还没有广泛应用于临床,但各界人士都开始相信并期待基因治疗技术可以从根源上去修正一些遗传缺陷,甚至可以赋予生命一些新的能力。基因治疗技术能够登上2017年《麻省理工科技评论》10大突破性技术榜单也恰恰证实了这一点。
但是挑战依然存在。基因治疗技术涉及多层次多领域,我们看到目前在疗效的考场上交上的最好成绩单的几类疾病都是单基因病,原因是单基因病的遗传缺陷明确而单一;而对于那些多基因调控的复杂疾病的认知还不足,即便有了很好的对基因进行操作的技术,却无用武之地。DNA的变异是无意识的,绝大部分变异并不与疾病相关,在上游从海量的突变中找到真正与疾病和表型相关的部分也是至关重要的一环。而下游基因治疗技术本身也存在着很多关键的技术难题,有待突破。外围的资本和监管也与基因治疗的推进和发展密切相关,美国Spark公司在2017年有一项针对罕见病的基因治疗技术有望获得FDA批准,而在我国红红火火的精准医疗市场上,大部分企业都在上游。基因治疗技术的开发和获益的周期长,风险大,资本市场的观望和目前监管的不健全都在一定程度上限制了技术的发展和应用。
我们看到基因治疗已经向世界展现了可行性,市场和患者的需求也十分强烈,基因治疗技术一定会给人类打开一扇全新的大门。这是一个了不起的时代,我们从未如此接近生命的密码。相信随着身处其中的各界人士的共同努力,中国的相关研究和应用也会稳步前进。
